醫療科技企業的凈利率排行榜單發布:心臟瓣膜介入治療釋放發展潛力
發布時間:2024-12-12 09:37
近日,LinkedIn(領英)公布了2023/2024全球醫療器械公司利潤率排名表。這張榜單展示了2023/2024財年全球主要醫療科技類公司的凈利潤率情況及排名。榜單上,排名前10的醫療科技公司分別為:邁瑞醫療、直覺醫療、愛德華、愛德士、瑞思邁、丹納赫、百特、聯影醫療、史賽克、德康,這些公司的凈利潤率均在14%以上,憑借較高的凈利潤率,往往在資本市場上也能獲得更高的市場估值,聚攏大量的資金。
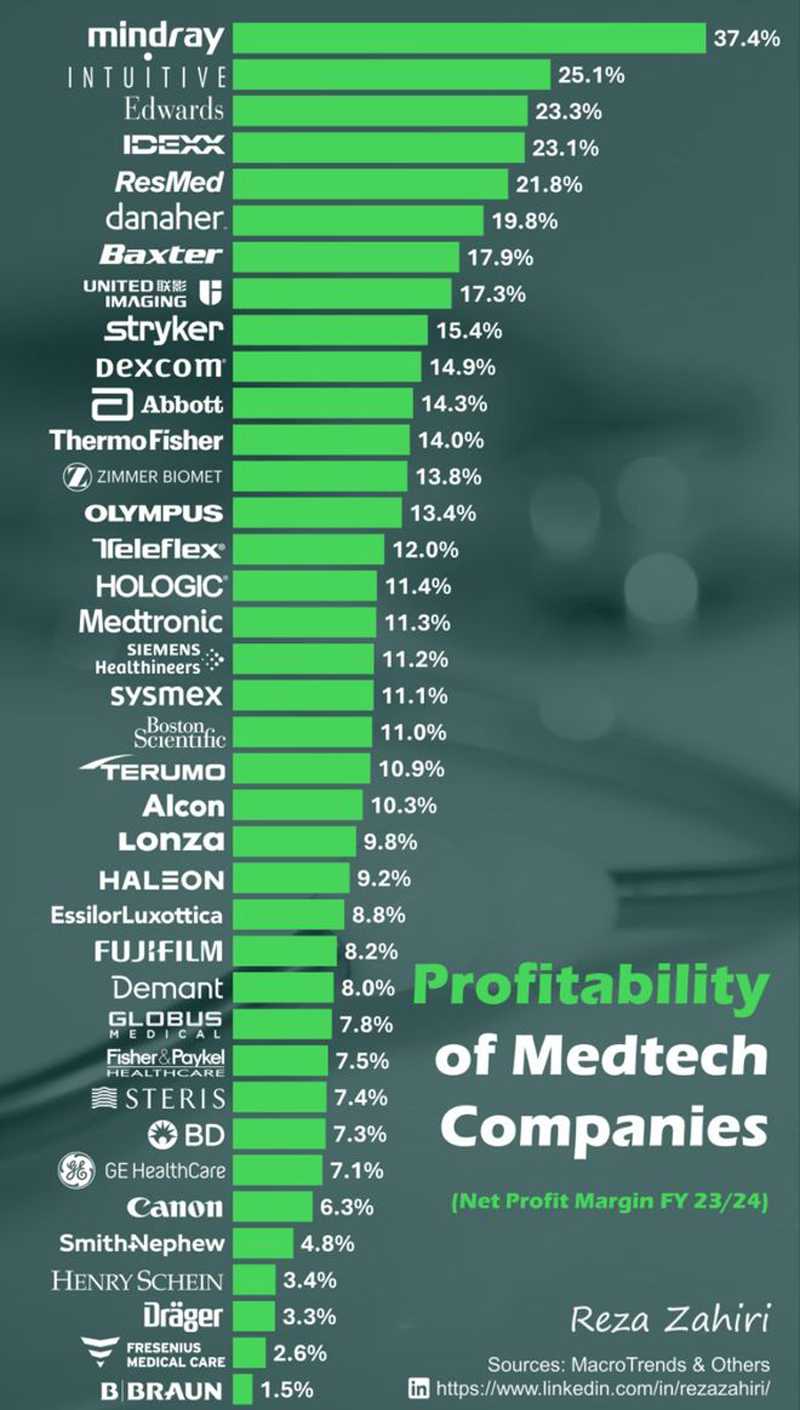
愛德華以23.3%的亮眼成績排名第三。眾所周知,在血管介入領域,愛德華一直以來以“心臟瓣膜之王”著稱。根據華爾街投資機構數據,2023年全球經導管主動脈瓣置換手術中愛德華的市場份額高達57.9%,遙遙領先于位居第二的美敦力(市場份額28.5%)。此外,榜單中雅培、波士頓科學同樣在心臟瓣膜領域有所耕耘和斬獲,該領域火熱程度可見一斑。
心臟瓣膜病(VHD)是全球心血管疾病發病和死忙的主要原因,微創介入治療越來越成為心臟瓣膜疾病治療的必然之路。心臟瓣膜微創介入領域,可以繼續細分為主動脈瓣、二尖瓣、三尖瓣、肺動脈瓣,根據相關數據,我國心臟瓣膜介入領域的市場規模預計在2030年可達420億元,年復合增長率(2023-2030年)約為45%。
隨著心臟瓣膜介入市場涌入大量資金后,國內介入領域的醫療科技企業,加速了在主動脈、肺動脈、二尖瓣、三尖瓣等細分領域的布局與開拓,紛紛加大研發投入,并逐步從模仿走向了創新。從相關數據統計與分析,可以窺見我國心臟瓣膜賽道的發展現狀、競爭格局與未來趨勢。
主動脈瓣介入領域
結構性心臟病2023年度報告披露,截至2023年11月末,中國TAVR(經導管主動脈瓣置換)手術共進行了1.36萬例,預估全年將超過1.5萬例,同比2022年增幅將超過77%,增速之快有目共睹。據統計,我國TAVRS手術始于2010年,從2010年到2022年底,過去十二年累計手術量僅有2.4萬例。
TAVR最初被應用于治療主動脈瓣狹窄(AS),隨后逐漸拓展到主動脈瓣反流(AR)治療領域。2023年11月,在中國心血管健康大會結構性心臟病介入論壇期間,《單純主動脈瓣反流經股動脈主動脈瓣置換中國專家共識2023》正式發布。自此之后,從AS推廣到AR,TAVR適應癥已擴展到手術低危患者,這意味著TAVR的適應患者數量將大大增加。
從市場規模來看,全球TAVR市場規模從2017年的34.7億美元增長至60.9億美元,預計到2030年還將高達158.9億美元,十年間復合增長率為11.2%。而在中國,TAVR市場規模從2017年的4000萬元增至2021年的9.1億元,預計到2030年將達到113.6億元,十年間復合增長率高達32.4%,增長速度急劇膨脹,遠高于全球水平。
在國內市場,TAVR領域目前進口與國產并行的局面,跨國企業為愛德華、美敦力,其余四家為國產企業,其中三家國產企業均已商業化至第二代產品。就細分賽道而言,目前主動脈瓣膜發展最為成熟、發展速度最快。
有數據顯示,截至2023年底,國內共有10款經導管主動脈瓣膜產品獲批NMPA,其中包含來自愛德華、美敦力,其余均為國產產品。因愛德華和美敦力的TAVR產品高于國產近40%,2023年國產TAVR產品領跑國內市場,四家國產廠商合計約占80%的植入份額。此外,還有多家國產企業入局該領域,除了已上市的產品,國內還有超過10家企業的研發管線中設置了TAVR產品,等待進入市場,競爭態勢在加劇中。
二尖瓣介入領域
TMV(二尖瓣介入治療)全球市場發展較早,且增長速度不斷加快,截至2023年已累計植入22萬例。而我國則起步較晚,2021年才出現商業化產品,截至2023年累計植入僅為1811例。
二尖瓣反流治療不及時將嚴重危害患者生命,隨著病情惡化會發展為心力衰竭和死亡。據統計,重癥二尖瓣反流1年死亡率高達57%。目前,外科手術是治療的金標準,但是超過50%的中度二尖瓣反流患者因年齡和合并癥等原因無法接受手術治療。根據相關推斷,我國成人中度及以上二尖瓣反流(MR)人群數量超過1700萬人,且市場供需缺口明顯,TMV空間巨大。
從市場規模來看,我國經導管二尖瓣介入治療市場規模預計將從2021年的3900萬元增加至2025年的17.35億元,復合增長率為156.8%,預計到2030年將達到89.43億元人民幣。
二尖瓣反流介入治療可以分為修復與置換路徑,其中修復(TEER)更為成熟。目前,全球共有9款二尖瓣介入治療器械獲得批準。TEER領域中,雅培的MitraClip是唯一一款獲得FDA/CE/NMPA三方認證的TMVr產品。愛德華的PASCAL也已獲得CE/FDA認證。國產方面,兩家企業的兩款產品獲得NMPA批準上市,打破了中國市場被外資壟斷的局面。
在二尖瓣置換領域,目前僅有雅培的經心尖入路Tendyne一款產品獲批CE,但臨床上存在諸多風險,在推廣上受到很大限制,市場存在一定空白。愛德華的Sapien M3展現了良好的安全性和有效性數據,預計不遠的將來會拿到CE認證。而國產方面,也有諸多公司入局該領域,但目前還沒有國產產品獲批上市。
由于安全問題的阻礙,介入置換器械商業化進程發展較緩,多款產品的術后一年死亡率都高達20%至30%。如果未來能夠有效解決安全性問題,置換類產品相對較低的操作難度、較短的手術時間和更徹底的反流干預效果或許能夠助力置換類產品成為二尖瓣疾病的主流治療器械。
三尖瓣介入領域
全球三尖瓣反流(TR)患者人數僅次于二尖瓣反流患者,超過了主動脈狹窄患者。國內方面,三尖瓣患者人數也僅次于二尖瓣患者,預計未來將影響約990萬人口。2021年至2030年,全球經導管三尖瓣介入手術量將從340例增長到45萬例,三尖瓣介入器械市場規模將從0.1億美元增長至112.8億美元,年復合增長率達118.35%。國內方面,2023年至2030年三尖瓣介入器械整體市場將從0.9億元增長至203.1億元,年復合增長率達118.44%,預計2030年國內三尖瓣介入手術將達到20萬例。
不完全統計,全球目前已經有11款三尖瓣介入治療產品,包括修復(TTVr)和置換(TTVR),大多處于在研階段。雅培的Tri Clip于2024年4月獲得FDA批準,為首款獲批FDA的經導管三尖瓣修復產品。愛德華的EVOQUE系統于2023年10月獲得CE批準,2024年2月獲得FDA批準,成為首個獲得FDA上市批準的經導管三尖瓣置換產品。目前,全球范圍內暫無產品獲得中國NMPA批準上市。國產方面,在研產品有4款,進度較快的產品處于確證性臨床試驗階段。
總的來說,雖然三尖瓣患者較多,但是目前上市產品較少,因此市場規模較小。此外,國內外大多數產品均處于臨床研究階段,預計將來隨著越來越多的產品上市,或許市場潛力會逐漸釋放。(圖片來自網絡,如有侵權請聯系刪除)
推薦新聞

2024政府工作報告——醫療衛生領域的相關內容來了!
- 2024-04-11

11家中國企業上榜2023全球醫療器械企業TOP100
- 2024-04-26
七八百元的集采心臟支架敢用嗎?國家醫保局用數據說話!
- 2024-04-11

國家醫保局:深化醫療服務價格改革,試點新增3省份
- 2024-03-20







